A Cara Therapeutics és üzleti partnere, a Vifor Pharma már 2021. augusztus 24-én bejelentette, hogy az FDA jóváhagyta első kategóriájában kappa opioid receptor agonista difelikefalinját (KORSUVA™) krónikus vesebetegségben (CKD) szenvedő betegek (pozitív közepes/súlyos viszketés hemodialízis kezelés mellett) kezelésére, és várhatóan 2022 első negyedévében kerül forgalomba. A Cara és a Vifor kizárólagos licencszerződést írt alá a KORSUVA™ Egyesült Államokban történő forgalmazására, és megállapodtak a KORSUVA™ Fresenius Medicalnak történő értékesítésében. Közülük a Cara és a Vifor egyenként 60%, illetve 40%-os profitrészesedéssel rendelkezik a Fresenius Medicalon kívüli árbevételből; mindkettő 50%-os profitrészesedéssel rendelkezik a Fresenius Medicaltól származó árbevételből.
A krónikus vesebetegséghez társuló pruritus (CKD-aP) egy generalizált pruritus, amely nagy gyakorisággal és intenzitással jelentkezik dialízisben részesülő krónikus vesebetegeknél. A pruritus a dialízisben részesülő betegek körülbelül 60-70%-ánál fordul elő, akik közül 30-40%-nál közepes/súlyos pruritus jelentkezik, ami komolyan befolyásolja az életminőséget (pl. rossz alvásminőség), és depresszióval jár. A krónikus vesebetegséghez társuló pruritusra korábban nem létezett hatékony kezelés, és a Difelikefalin jóváhagyása segít áthidalni a hatalmas orvosi szükséglethiányt. Ez az engedélyezés két, az NDA bejelentésében szereplő, III. fázisú, pivotális klinikai vizsgálaton alapul: a KALM-1 és KALM-2 vizsgálatok pozitív adatain az Egyesült Államokban és világszerte, valamint 32 további klinikai vizsgálat alátámasztó adatain, amelyek azt mutatják, hogy a KORSUVA™ jól tolerálható.
Nemrégiben jó hírek érkeztek a difelikefalin japán klinikai vizsgálatából: 2022. január 10-én a Cara bejelentette, hogy partnerei, a Maruishi Pharma és a Kissey Pharma megerősítették, hogy a difelikefalin injekciót Japánban alkalmazzák a hemodialízisben részesülő betegek viszketésének kezelésére. III. fázisú klinikai vizsgálatok Az elsődleges végpont teljesült. 178 beteg kapott 6 hétig difelikefalint vagy placebót, és részt vett egy 52 hetes, nyílt, kiterjesztett vizsgálatban. Az elsődleges végpont (a viszketés numerikus értékelő skáláján elért pontszám változása) és a másodlagos végpont (a viszketés pontszámának változása a Shiratori Súlyossági Skálán) szignifikánsan javult a kiindulási értékhez képest a difelikefalin csoportban a placebo csoporthoz képest, és a betegek jól tolerálhatók voltak.
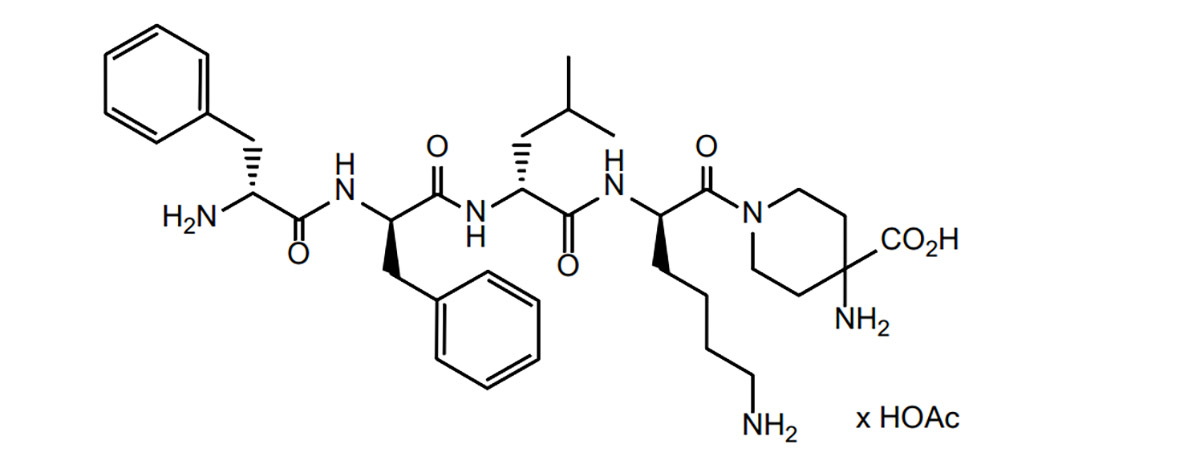
A difelikefalin az opioid peptidek egyik osztálya. Ennek alapján a Peptid Kutatóintézet tanulmányozta az opioid peptidekkel kapcsolatos szakirodalmat, és összefoglalta az opioid peptidek gyógyszerfejlesztési nehézségeit és stratégiáit, valamint a jelenlegi gyógyszerfejlesztési helyzetet.
Közzététel ideje: 2022. február 17.